間充質(zhì)幹細胞(MSCs)是一種多(duō)能(néng)幹細胞,可(kě)從多(duō)種組織來源中(zhōng)分(fēn)離得到,最常見的為(wèi)骨髓、脂肪組織和臍帶。MSCs具(jù)有(yǒu)自我更新(xīn)能(néng)力,并可(kě)被誘導分(fēn)化為(wèi)脂肪、軟骨、骨、肝、肌腱和心肌等多(duō)種類型的細胞。MSCs可(kě)通過抑制T細胞和淋巴細胞增殖等機制調節免疫反應[1, 2]。此外,MSCs還具(jù)有(yǒu)抗氧化、抗凋亡、抗纖維化和促血管生成的特性[8]。因此,MSCs在免疫調節和組織再生方面具(jù)有(yǒu)顯著的臨床潛力。事實上,MSCs已在許多(duō)臨床試驗中(zhōng)用(yòng)于免疫介導疾病和組織損傷的治療。已使用(yòng)MSCs治療的疾病包括肝病、周圍神經損傷、移植物(wù)抗宿主病、自身免疫性疾病、糖尿病和心髒病[3, 4]。2024年12月18日,美國(guó)食品藥品監督管理(lǐ)局(FDA)批準Ryoncil(remestemcel-L-rknd)上市,這是一種異體(tǐ)間充質(zhì)基細胞療法(mesenchymal stromal cell,MSC),用(yòng)于治療對類固醇無反應的急性移植物(wù)抗宿主病(SR-aGVHD),适用(yòng)于年齡為(wèi)2個月及以上的兒科(kē)患者。
臨床需求
MSCs在治療應用(yòng)中(zhōng)的一個關鍵限制是其在所有(yǒu)組織中(zhōng)的數量都很(hěn)少,且分(fēn)離得到的MSCs數量不足以滿足臨床需求。通常給予患者的劑量為(wèi)2 × 106 cells/kg體(tǐ)重[1, 2]。對于某些患者和疾病,為(wèi)達到所需的治療效果,需要多(duō)次給予多(duō)達數億個MSCs[5, 6]。雖然傳統的細胞培養皿和培養瓶在體(tǐ)外擴增MSCs,也可(kě)以獲得實驗級别足夠細胞數量,但對于臨床用(yòng)途而言遠(yuǎn)遠(yuǎn)不夠。如使用(yòng)細胞培養瓶進行大規模細胞擴增時,需要更多(duō)的人力和培養空間。此外,使用(yòng)細胞培養瓶進行大規模擴增不僅效率低下,而且還會影響細胞質(zhì)量,因為(wèi)長(cháng)期在體(tǐ)外擴增的MSCs可(kě)能(néng)會失去其幹細胞特性[7]。既往研究還報告稱,當MSCs達到較高的傳代次數時,其增殖和分(fēn)化潛力會降低[8]。因此,确定一種有(yǒu)效的大規模擴增技(jì )術對于在短時間内以具(jù)有(yǒu)成本效益的方式獲得大量細胞,同時不損害細胞質(zhì)量而言至關重要。
常見規模化擴增工(gōng)藝
目前MSCs的大規模擴增主要有(yǒu)4種策略,即多(duō)層細胞工(gōng)廠、轉瓶(spinner)、滾瓶(roller bottle)和生物(wù)反應器。四種方法各有(yǒu)優劣。
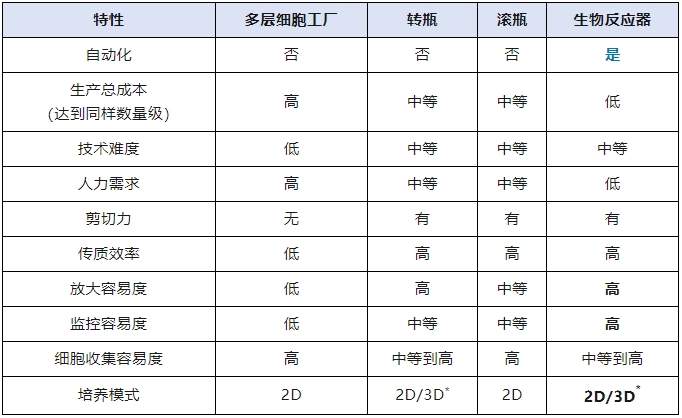
*本文(wén)中(zhōng)的2D培養指細胞貼附在培養容器表面培養,3D培養指在多(duō)孔微載體(tǐ)上培養,而在實心微載體(tǐ)表面培養則被認為(wèi)是介于2D和3D之間。
工(gōng)藝選擇的主要考量點
✦ 生産(chǎn)效率和成本:轉瓶和滾瓶可(kě)以被視作(zuò)簡化版的迷你生物(wù)反應器,但和多(duō)層細胞工(gōng)廠一樣,都需要大量的人工(gōng)操作(zuò),而且比細胞工(gōng)廠占用(yòng)更多(duō)的場地。生物(wù)反應器則能(néng)實現自動化3D培養,占據的車(chē)間面積大大減少。
✦ 生産(chǎn)效率和成本:轉瓶和滾瓶可(kě)以被視作(zuò)簡化版的迷你生物(wù)反應器,但和多(duō)層細胞工(gōng)廠一樣,都需要大量的人工(gōng)操作(zuò),而且比細胞工(gōng)廠占用(yòng)更多(duō)的場地。生物(wù)反應器則能(néng)實現自動化3D培養,占據的車(chē)間面積大大減少。
✦ 規模和難度:較小(xiǎo)的培養容器僅适合于擴增自體(tǐ)回輸用(yòng)MSCs,而不足以滿足每批生産(chǎn)可(kě)産(chǎn)生多(duō)人份的異體(tǐ)治療劑量需求。生物(wù)反應器因其可(kě)控的培養環境,更利于大規模MSCs的擴增,而不會影響細胞活力、表面标記物(wù)表達和分(fēn)化潛力。但操作(zuò)起來技(jì )術門檻較高,需要技(jì )術人員具(jù)備一定經驗。
✦ 表面marker:生物(wù)反應器擴增後CD105的陽性表達率降至95%以下(BM-MSCs為(wèi)88%,AT-MSCs為(wèi)92%)[9]。其他(tā)幾項研究也報道了使用(yòng)生物(wù)反應器和轉瓶擴增的MSCs上CD90和CD105的表達減少[10,11]。作(zuò)者推測,這可(kě)能(néng)是由于剪切力或消化過程引起的細胞損傷。據報道,與CD105+ MSCs相比,CD105- MSCs更容易分(fēn)化為(wèi)脂肪細胞和骨細胞,并且更有(yǒu)效地抑制CD4+ T細胞的增殖,但心髒再生潛力卻更差。CD90- MSCs與較弱的免疫抑制活性和增強的成骨和脂肪基因分(fēn)化有(yǒu)關[12,13]。因此,在生物(wù)反應器和轉瓶擴增後CD90和CD105表達的缺失可(kě)能(néng)會增強MSCs治療癌症某些疾病的效力。
✦ 擴增倍數:根據Hassan等人的統計分(fēn)析,目前所報道的生物(wù)反應器和細胞工(gōng)廠的擴增倍數要比轉瓶和滾瓶要高。對于細胞工(gōng)廠,不同研究的擴增倍數比差異很(hěn)大,一些研究報告的擴增倍數低于20倍,但有(yǒu)少數研究報告的擴增倍數超過100倍,可(kě)能(néng)是種子初始密度較低所緻[1]。
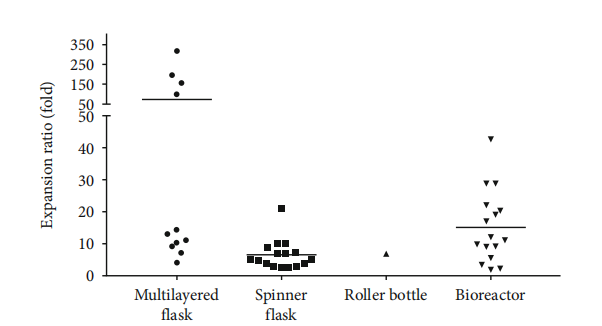
使用(yòng)不同的生物(wù)工(gōng)藝獲得的擴增率[14]
賽科(kē)成MSCs大規模培養方案:
賽科(kē)成在貼壁細胞培養方面有(yǒu)多(duō)年經驗積累,在内部測試及客戶現場均獲得了良好的結果。市面上微載體(tǐ)一般分(fēn)為(wèi)可(kě)降解與不可(kě)降解兩種。針對這兩種不同工(gōng)藝,賽科(kē)成均有(yǒu)對應的全套解決方案。

工(gōng)藝路線(xiàn)1:适用(yòng)于可(kě)降解型球狀微載體(tǐ)
細胞可(kě)降解型球狀微載體(tǐ)表面及孔洞内部進行,是一種更接近于天然組織中(zhōng)3D培養的模式。對MSCs進行擴增,可(kě)以配合賽科(kē)成玻璃罐體(tǐ)反應器或一次性攪拌式反應器進行擴增,在反應器内完成細胞的貼壁、培養和微載體(tǐ)酶解步驟,并支持逐級放大,最多(duō)可(kě)以放大至三級,單批次生産(chǎn)百億量級MSCs。
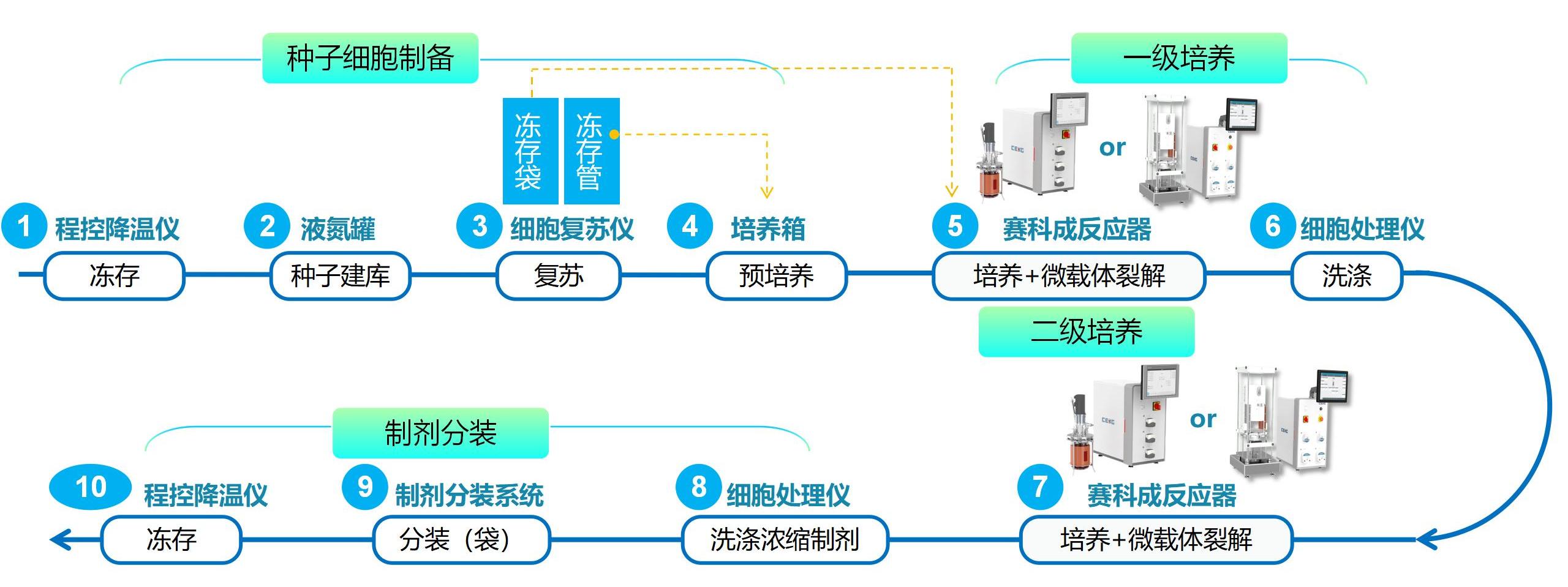
工(gōng)藝路線(xiàn)2:适用(yòng)于不可(kě)降解型2D微載體(tǐ)
MSCs在不降解型2D微載體(tǐ)表面進行擴增,是一種介于2D和3D之間的培養方式,擴增完成後需要用(yòng)重組胰酶等消化液進行消化,才能(néng)進行細胞的收獲或進一步放大培養。可(kě)以配合賽科(kē)成玻璃罐體(tǐ)反應器或一次性攪拌式反應器進行擴增,在反應器内完成細胞的貼壁和培養,然後轉移到專有(yǒu)的微載體(tǐ)消化清洗罐内進行消化和清洗。同樣支持逐級放大,最多(duō)可(kě)以放大至三級,單批次生産(chǎn)百億量級MSCs。
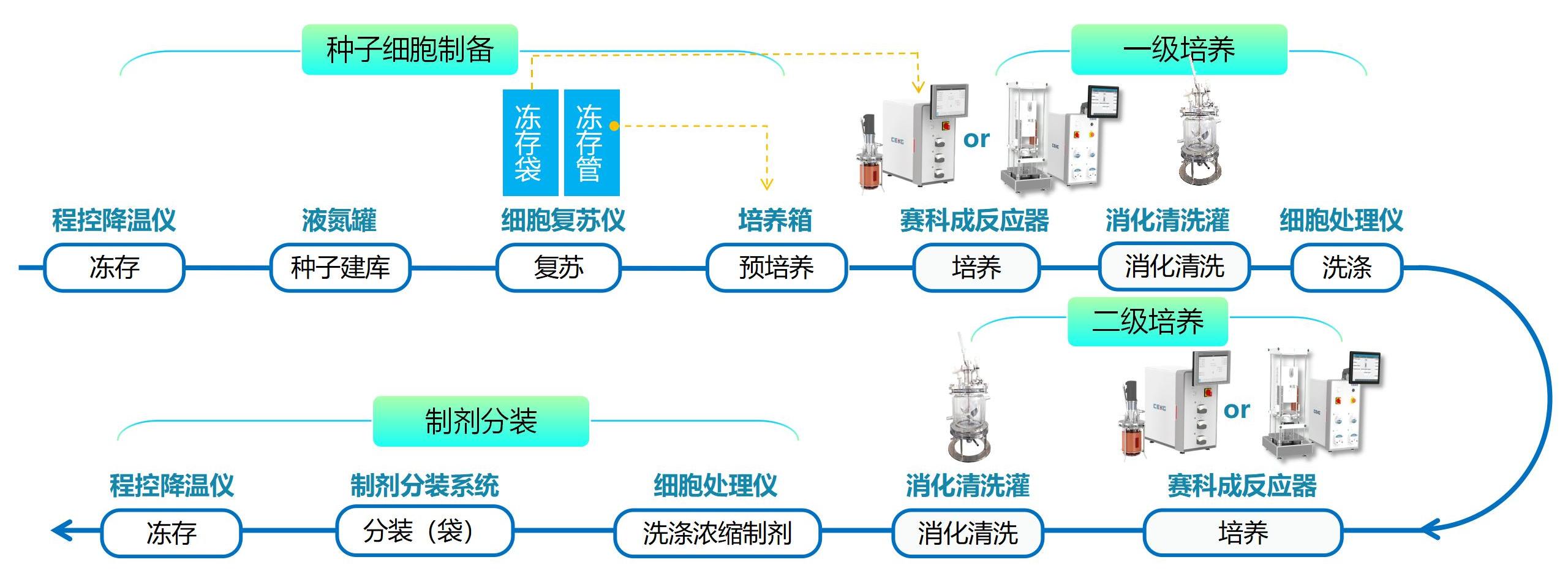
賽科(kē)成生物(wù)反應器
賽科(kē)成有(yǒu)多(duō)種型号規格的生物(wù)反應器,并可(kě)以提供相應技(jì )術方案,支持MSCs培養中(zhōng)培養基、微載體(tǐ)的篩選及工(gōng)藝優化,小(xiǎo)試至大規模擴增工(gōng)藝全流程。

參考文(wén)獻:
[1] Usha, Nekanti, and, Lipsa, Mohanty, & and, et al. (2010). Optimization and scale-up of wharton's jelly-derived mesenchymal stem cells for clinical applications. Stem Cell Research.
[2] Caruso, S. R. , Orellana, M. D. , Mizukami, A. , Fernandes, T. R. , Fontes, A. M. , & Suazo, C. A. T. , et al. (2014). Growth and functional harvesting of human mesenchymal stromal cells cultured on a microcarrier‐based system. Biotechnology Progress, 30(4), 889-895.
[3] Watson, N. , Divers, R. , Kedar, R. , Mehindru, A. , Mehindru, A. , & Borlongan, M. C. , et al. (2015). Discarded wharton jelly of the human umbilical cord: a viable source for mesenchymal stromal cells. Cytotherapy, 17( 1), 18-24.
[4] Guan, L. , Guan, H. , Li, H. , Ren, C. , Liu, L. , & Chu, J. , et al. (2015). Therapeutic efficacy of umbilical cord-derived mesenchymal stem cells in patients with type 2 diabetes. Experimental & Therapeutic Medicine.
[5] El-Kheir, W. A. , Gabr, H. , Awad, M. R. , Ghannam, O. , Barakat, Y. , & Farghali, H. A. M. A. , et al. (2014). Autologous bone marrow-derived cell therapy combined with physical therapy induces functional improvement in chronic spinal cord injury patients. Cell Transplantation, 23(6), 729-45.
[6] J. Vaquero, M. Zurita, M. A. Rico et al.(2018), Intrathecal administration of autologous mesenchymal stromal cells for spinal cord injury: safety and efficacy of the 100/3 guideline,Cytotherapy 20(6),806–819
[7] Bonab, M. M. , Alimoghaddam, K. , Talebian, F. , Ghaffari, S. H. , Ghavamzadeh, A. , & Nikbin, B. . (2006). Aging of mesenchymal stem cell in vitro. BMC Cell Biology, 7(1), 1-7.
[8] (2012). Large-scale production of human mesenchymal stem cells for clinical applications. Biotechnology & Applied Biochemistry, 59(2), 106-120.
[9] B. Cunha, T. Aguiar, S. B. Carvalho et al.(2017), Bioprocess integration for human mesenchymal stem cells: from up to ownstream processing scale-up to cell proteome characterization, Journal of Biotechnology 248, 87–98.
[10] Patrícia Aparecida, Tozetti, Rigotto, S. , Caruso, Amanda, & Mizukami, et al. (2017). Expansion strategies for human mesenchymal stromal cells culture under xeno-free conditions. Biotechnology progress.
[11] F. dos Santos, A. Campbell, A. Fernandes-Platzgummer et al. (2014), A xenogeneic-free bioreactor system for the clinical-scale expansion of human mesenchymal stem/stromal cells, Biotechnology and Bioengineering 111(6) 1116– 1127.
[12] Campioni,D.,Rizzo,R.,Stignani,M.,Melchiorri,L.,Ferrari,L.,&Moretti,S.,etal.(2010).Adecreased positivity for cd90 on human mesenchymal stromal cells(mscs)isassociated with a loss of immunosuppressiveactivity by mscs.Cytometry Part BClinical Cytometry,76B(3), 225-230.
[13] Moraes, D.A.,Sibov,T.T.,Pavon,L.F.,Alvim,P.Q.,Bonadio,R.S.,&DaSilva,J.R.,etal.(2016).Areductionincd90(thy-1)expression results in increased differentiation of mesenchymal stromal cells.Stem CellResearch&Therapy, 7(1).
[14] Hassan, M. N. F. B. , Yazid, M. D. , Yunus, M. H. M. , Chowdhury, S. R. , & Law, J. X. . (2020). Large-scale expansion of human mesenchymal stem cells. Stem Cells International, 2020(1), 1-17.
如果您有(yǒu)更多(duō)需求,點擊按鈕,提交信息,我們會第一時間給您回複。
If you have more requirements, click the button to submit information, and we will reply to you as soon as possible.
版權所有(yǒu) © 2025 All Rights Reserved. 武漢賽科(kē)成科(kē)技(jì )有(yǒu)限公(gōng)司 京ICP證000000号 網站建設:烽虎網絡